Trong bài học về hóa trị, chúng ta thường gặp gốc CO3 xuất hiện trong các công thức như CaCO3, Na2CO3, H2CO3. Vậy CO3 là gốc gì? CO3 hóa trị mấy? Nhóm kèm CO3 hóa trị bao nhiêu? Bài viết này sẽ giúp các bạn hiểu rõ hơn về CO3, bao gồm tính chất, công dụng và cách điều chế.
Nội dung
CO3 là gốc gì?
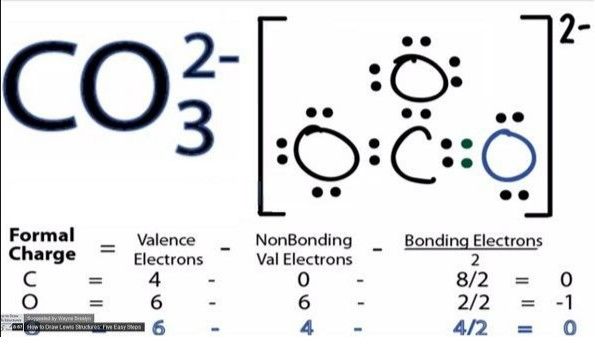
CO3 thực chất là một gốc thuộc Acid carbonic, còn được gọi là gốc Ca-bừn-nết khi đọc tên các hợp chất muối có gốc CO3. Khi CO3 không nằm trong bất kỳ hợp chất muối nào, ta đọc là Carbon trioxide.
Trong đó, Acid carbonic là một acid yếu với công thức hóa học là H2CO3. Acid carbonic tạo ra hai loại muối: Carbonate và Bicarbonate.
CO3 hóa trị mấy?
Cấu trúc của Carbonate tuân theo quy tắc octet, do đó oxygen cũng mang dấu âm. Hóa trị là số lượng liên kết hình thành bởi nguyên tử, dẫn đến hình thành hợp chất.
Carbonate có thể kết hợp với hai nguyên tử Hydrogen theo công thức hóa học của acid carbonic H2CO3, ta có thể xác định hóa trị như sau:
H2CO3 có Hydrogen mang hóa trị I và gọi a là hóa trị của CO3.
Công thức quy tắc:
1.2 = a.1 => a = 2
Vậy có thể kết luận gốc CO3 mang hóa trị II. Khối lượng mol và khối lượng phân tử CO3 đều là 60,009.
Cách điều chế CO3
Việc điều chế CO3 khá đơn giản bằng cách thổi một luồng không khí vào trong nước sạch. Tuy nhiên, phương thức này có thể tạo ra sự khác biệt.
Phương trình phản ứng điều chế:
CO2 + H2O -> H2CO3
Các loại hợp chất thường thấy của CO3
Có hai loại hợp chất chính của CO3, đó là acid carbonic và muối Carbonate.
Hợp chất axit Carbonic – H2CO3
Tính chất vật lý:
- Khí carbon dioxide tan trong nước và nước mưa. Mỗi 1000m3 nước trung bình tan 90m3 CO2.
- Phần lớn CO2 tác dụng với nước tạo thành dung dịch acid carbonic, tồn tại dưới dạng phân tử CO2.
Tính chất hóa học:
- H2CO3 là một acid yếu, dung dịch làm quỳ tím chuyển đỏ nhạt và bị acid mạnh đẩy ra khỏi muối.
- H2CO3 là một acid không bền, dung dịch tạo thành trong các phản ứng hóa học sau đó bị phân hủy thành CO2 và H2O.
Hợp chất muối Carbonat
Muối Carbonate chia làm 2 loại: muối Carbonate trung hòa và muối Carbonate acid (muối hidrocarbonate).
Muối Carbonate trung hòa: Sodium Carbonate (Na2CO3), Magnesium carbonate, Calcium Carbonate (CaCO3).
Muối Carbonate acid: Sodium Bicarbonate (NaHCO3), Calcium Bicarbonate (Ca(HCO3)2), Potassium bicarbonate (KHCO3).
Tính tan của muối Carbonate:
- Đa số muối Carbonate không tan trong nước, trừ các muối của kim loại kiềm như Na2CO3, K2CO3…
- Các muối hidrocarbonate đều tan trong nước, ví dụ như Mg(HCO3)2 và Ca(HCO3)2.
Tính chất hóa học của muối Carbonate:
- Muối Carbonate tác dụng với dung dịch acid mạnh như HCl, H2SO4 và HNO3 để tạo ra muối mới và CO2.
- Một số dung dịch muối Carbonate khác tác dụng với dung dịch base để tạo ra muối mới và base mới.
- Dung dịch muối Carbonate tác dụng với một số dung dịch muối thông qua phản ứng tạo ra hai muối mới.
- Ngoài ra, nhiều muối Carbonate có khả năng phân hủy và giải phóng khí CO2.
Muối Carbonate được ứng dụng rộng rãi trong đời sống và sản xuất công nghiệp. Mỗi loại muối Carbonate đều có tính chất ứng dụng riêng.
- Calcium Carbonate (CaCO3) dùng để sản xuất xi măng, vôi, xây dựng và ngành sơn.
- Sodium Carbonate (Na2CO3) dùng để sản xuất thủy tinh, xà phòng và hóa chất gốc sodium.
- Sodium Bicarbonate (NaHCO3) được sử dụng trong ẩm thực, làm đẹp, dược phẩm và chữa bệnh dạ dày.
Cách nhận biết ion Carbonate
Để nhận biết ion Carbonate, ta có thể cho tác dụng với dung dịch acid. Nếu tạo hiện tượng sủi bọt khí CO2, đó là ion Carbonate.
Phương trình phản ứng:
CaCO3 + 2HCl -> CaCl2 + CO2 + H2O
Một số ứng dụng của muối Carbonate
CO3 đề cập đến ion Carbonate (CO32-), có nhiều ứng dụng quan trọng trong các lĩnh vực khác nhau.
- Calcium Carbonate (CaCO3): Được sử dụng trong xây dựng, xi măng, sơn và ngành công nghiệp.
- Sodium carbonate (Na2CO3): Nguyên liệu chính trong sản xuất thủy tinh, xà phòng và hóa chất gốc sodium.
- Sodium Bicarbonate (NaHCO3): Sử dụng trong ẩm thực, làm đẹp, dược phẩm và chữa bệnh dạ dày.
Hy vọng bài viết này đã giúp bạn hiểu rõ hơn về CO3 – gốc Acid Carbonic. Mong rằng thông tin này sẽ giúp bạn nắm bắt kiến thức và nâng cao kết quả học tập.